作为真核生物DNA上的一种重要表观遗传修饰,DNA N6-甲基腺嘌呤(6mA)已被证实在应激响应、胚胎发育及免疫调控等多种生物学过程中扮演关键角色。单细胞真核生物的6mA含量尤其丰富,且有明确的6mA“书写器”(AMT1甲基转移酶复合体)在ApT基序上建立和维持6mA。然而,一个长期悬而未决的问题是:单细胞真核生物中负责6mA去除的“橡皮擦”(去甲基化酶)究竟是谁?它们又发挥着怎样的生物学功能?
近日,高珊教授课题组在PNAS杂志发表题为“A distinct subclade of AlkB family demethylases in ciliates safeguards the positional fidelity of eukaryotic N6-methyladenine (6mA)”(纤毛虫独特的AlkB家族去甲基化酶维持6mA的准确定位)的研究成果,为这个谜题提供了答案。该研究在单细胞模式生物——嗜热四膜虫中,鉴定并解码了首个6mA去甲基化酶DMT3的作用机制,揭示了其与多细胞生物同源蛋白不同的催化特性,以及其在调控基因表达、保障有性生殖启动过程中的关键作用。

在本研究中,团队首先通过系统发育分析,在嗜热四膜虫中找到一个AlkB家族ALKBH5分支的同源蛋白DMT3(图1A),并通过一系列遗传学和分子生物学实验证实了它的身份:DMT3敲除导致全基因组6mA水平显著升高约20%(图1B),伴随大量异常甲基化位点的出现(图1C),并导致6mA去甲基化中间产物6hmA的水平显著降低(图1D);将AlkB家族保守的Fe2+离子和α-酮戊二酸结合基序突变的DMT3回补至DMT3敲除株系后,6mA水平无法恢复(图1E)。这一系列证据证明,DMT3是一个关键的6mA去甲基化酶。
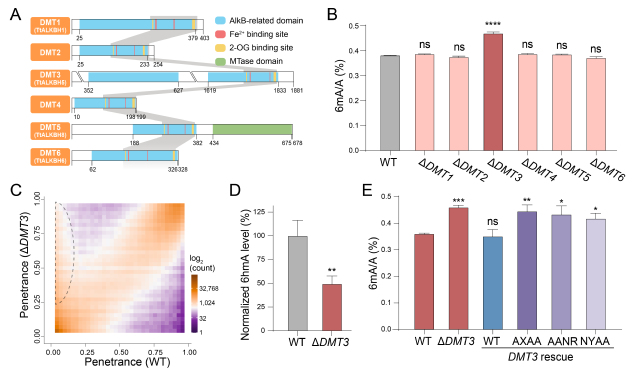
图1. DMT3是6mA去甲基化酶。(A)DMT1-6具有AlkB家族的保守结构域;(B)DMT3敲除株系整体6mA水平显著上升;(C)DMT3敲除株系中部分腺嘌呤位点的6mA水平显著上升;(D)DMT3敲除株系的6hmA水平显著下降;(E)野生型DMT3回补使6mA水平恢复,而突变DMT3回补则不能使6mA水平恢复。
与多细胞真核生物中主要作用于单链RNA m6A修饰的ALKBH5同源蛋白不同,DMT3特异性地靶向双链DNA上的对称ApT基序,并且能作用于全甲基化和半甲基化状态的6mApT位点(图2A-C)。研究进一步发现,DMT3对双链DNA的偏好性可能源于其催化结构域中一个关键的天然氨基酸替换(半胱氨酸到丝氨酸),该氨基酸替换在整个纤毛虫谱系中普遍存在(图2D)。将该位点反向突变为半胱氨酸会显著削弱其对双链DNA 6mA的去甲基化能力(图2E)。
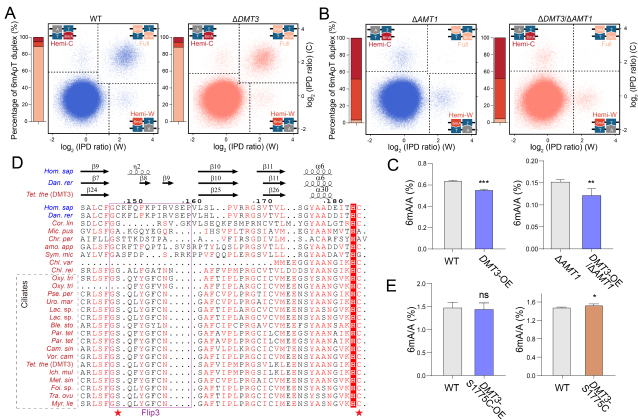
图2. DMT3作用于全甲基化和半甲基化的6mApT。(A)野生型和DMT3敲除株系的6mApT都主要是全甲基化状态;(B)AMT1敲除和AMT1、DMT3双敲除株系的6mApT都主要是半甲基化状态;(C)在野生型(全甲基化位点为主)和AMT1敲除(半甲基化状态为主)株系中过表达DMT3都能使6mA水平显著下降;(D)与多细胞动物ALKBH5同源蛋白相比,纤毛虫ALKBH5同源蛋白的Flip3区域存在天然的半胱氨酸到丝氨酸的替换;(E)DMT3-S1775C过表达不能使6mA显著下降,DMT3-S1775C突变使6mA显著上升。
在野生型细胞中,AMT1甲基转移酶复合体主要负责在转录起始位点(TSS)下游的基因区添加6mA,而DMT3则特异性地驻留在TSS区域,清除被AMT1错误添加到该区域的6mA。当DMT3缺失后,TSS区域会出现大量异常累积的6mA(图3A,B)。
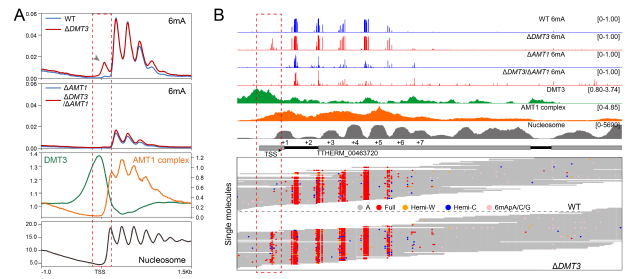
图3. DMT3去除AMT1在TSS处添加的6mA。(A)6mA、DMT3、AMT1复合体以及核小体的基因组分布特征;(B)代表性基因座的6mA、DMT3、AMT1复合体以及核小体分布特征。
与此同时,DMT3敲除株系的有性生殖(接合生殖)启动严重受阻(图4A,B)。分析发现,细胞配对所必需的MTA6、MTB6和CDK19基因的TSS区域出现异常6mA,并伴随局部染色质开放性下降和转录沉默(图4C)。而通过同时敲除甲基转移酶编码基因AMT1消除TSS区域的异常6mA后,接合生殖缺陷的表型被成功拯救(图3A,3B,4A)。这一结果清晰地表明,DMT3介导的6mA去甲基化,通过清除关键基因TSS区域的6mA“噪音”以维持正常转录,从而保障接合生殖正常启动。
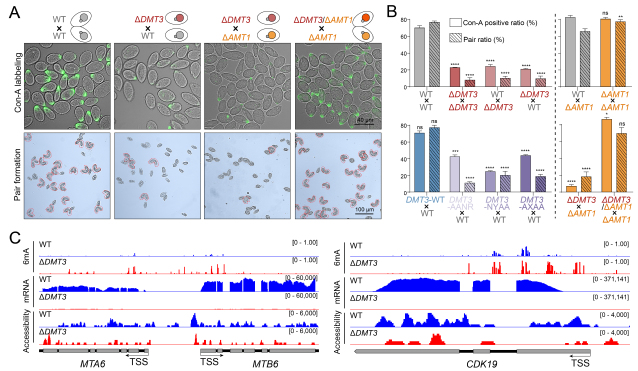
图4. DMT3参与调控四膜虫接合生殖启动。(A)DMT3敲除阻碍接合生殖启动,而AMT1与DMT3双敲除则又可以使这种接合生殖缺陷恢复;(B)各个株系配对组合的接合生殖启动效率统计;(C)MTA6、MTB6和CDK19基因座的6mA、转录以及染色质开放性状态。
综上所述,本研究在单细胞真核生物嗜热四膜虫中,首次鉴定出AlkB家族的6mA去甲基化酶DMT3,并揭示了其区别于多细胞生物同源蛋白的独特催化特性。研究提出的工作模型(图5)描绘了细胞如何利用AMT1(书写器)和DMT3(橡皮擦)在TSS区域构建“动态平衡”,从而确保6mA修饰的精准定位。这一发现不仅为单细胞真核生物的6mA去甲基化酶研究补上了关键一环,也为理解DNA修饰的位置准确性提供了重要切入点。
与此同时,本研究的发现也为系统性比较真核生物中两种主要的DNA甲基化修饰6mA与5-甲基胞嘧啶(5mC)提供了新的维度。传统观点认为,多细胞真核生物的5mC与单细胞真核生物的6mA功能相反:5mC与转录抑制相关,而6mA则与转录激活关联。然而,越来越多证据表明,启动子区域的5mC抑制转录,而基因内部的5mC常与活跃转录相关。单细胞真核生物中的6mA大多富集在TSS下游并发挥转录激活作用,而本研究发现TSS附近的异常6mA则倾向于抑制转录。因此,5mC与6mA或许并非如传统观点所认为的功能对立,而是可能遵循着相似的调控逻辑:DNA甲基化的转录效应取决于其在基因组中的位置。这一认识不仅深化了对6mA功能机制的理解,也为探讨DNA修饰在真核生物演化过程中的功能保守性与分化提供了全新视角。
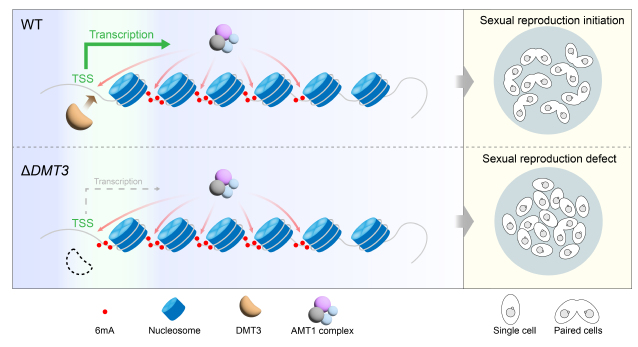
图5. DMT3表观遗传调控功能模式图。
该研究由中国海洋大学进化所原生动物学团队高珊教授课题组完成。高珊教授课题组博士生牛俊骅和于浩泽为该文章的共同第一作者,高珊教授为文章的通讯作者。高珊教授课题组博士毕业生刘永强,南北,博士生聂兰蘅,云南大学生物医药研究院章文信副教授,中国海洋大学医药学院宋妮老师,中科院分子细胞科学卓越创新中心荣少钦博士,复旦大学生物医学研究院周丹副研究员对该工作亦有重要贡献。

刘永强(第一排左一),于浩泽(第一排左四),牛俊骅(第一排右一),南北(第二排左二),聂兰蘅(第二排右一)。
原文链接:
www.pnas.org/doi/10.1073/pnas.2526398123
参考文献:
1. Xu, G.L., and Bochtler, M. Reversal of nucleobase methylation by dioxygenases. Nature Chemical Biology. 2020; 16: 1160-1169.
2. Wang, Y.Y., Sheng, Y.L., Liu, Y.Q., Zhang, W.X. et al. A distinct class of eukaryotic MT-A70 methyltransferases maintain symmetric DNA N6-adenine methylation at the ApT dinucleotides as an epigenetic mark associated with transcription. Nucleic Acids Research 2019; 47: 11771-89.
3. Beh, LY., Debelouchina, GT., Clay, DM., Thompson, RE. et al. Identification of a DNA N6-Adenine methyltransferase complex and its impact on chromatin organization. Cell 2019; 177: 1781-96.e25.
4. Cheng, T., Zhang, J.C., Li, H.C., Diao, J.H. et al. Identification and characterization of the de novo methyltransferases for eukaryotic N6-methyladenine (6mA). Science Advances 2025; 11: eadq4623.
5. Sheng, Y.L., Wang, Y.Y., Yang, W.T., Wang, X.Q. et al. Semiconservative transmission of DNA N6-adenine methylation in a unicellular eukaryote. Genome Research. 2024; 34: 740-756.
6. Zheng, G.Q., Dahl, JA, Niu, Y.M., Fedorcsak, P. et al. ALKBH5 is a mammalian RNA demethylase that impacts RNA metabolism and mouse fertility. Molecular Cell. 2013; 49: 18-29.
7. Li, H.C., Niu, J.H., Sheng, Y.L., Liu, Y.F. et al. SMAC: identifying DNA N6-methyladenine (6mA) at the single-molecule level using SMRT CCS data. Briefings in Bioinformatics. 2025; 26: bbaf153.


