上皮组织是构成人体器官的重要基础结构,其稳定性与动态重塑能力依赖于细胞之间的“黏附连接”。E-cadherin作为核心黏附分子,负责连接相邻细胞;F-actin则构成细胞骨架,参与力的产生与传递。长期以来,两者在细胞连接处的精细空间关系尚未被清晰解析。
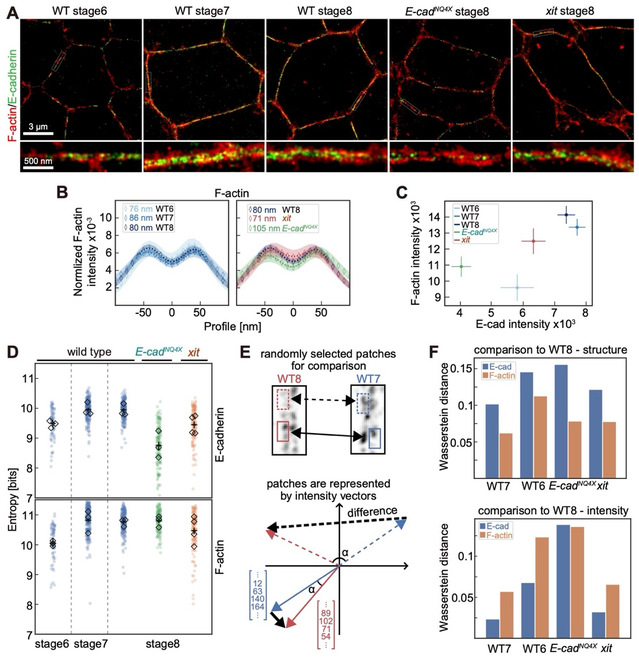
本研究采用DNA/peptide-PAINT超分辨显微技术,将成像精度提升至20纳米以内,成功分辨出细胞连接两侧E-cadherin纳米簇的空间分布。研究发现,E-cadherin在连接处形成“成对”与“未成对”两类纳米簇结构,且其空间排列随发育阶段发生变化。同时,研究团队发现,细胞两侧F-actin的组织相关性并不完全依赖E-cadherin的配对状态,提示细胞间力学整合机制可能比传统认识更加复杂。此外,研究还系统分析了E-cadherin的N-糖基化修饰对连接结构和力学性质的影响。结果表明,糖基化状态改变会影响纳米簇的配对比例和分布特征,并对细胞连接的力学行为产生调控作用。
本研究在技术层面建立了适用于厚组织成像的DNA-PAINT应用方案,在理论层面深化了对细胞黏附与细胞骨架协同机制的理解,对揭示组织形态发生、生物力学调控及相关疾病机制具有重要意义。

该成果以题为《DNA-PAINT resolves E-cadherin-independent cross-junctional F-actin organization in Drosophila embryonic tissue》的研究长文发表在美国生物物理学会旗舰刊物《Biophysical Journal》,并被选为当期封面文章。作者受邀在美国生物物理学会网站配发题为“Nanoscale Insights: Unveiling the Architecture of Adherens Junctions in Tissue”介绍(https://www.biophysics.org/blog/nanoscale-insights-unveiling-the-architecture-of-adherens-junctions-in-tissue)。
孔德清教授、德国马尔堡大学Jörg Großhans教授和德国哥廷根大学Fred Wolf教授为共同通讯作者,英国剑桥大学Daniel St Johnston院士有重要贡献。
全文链接:https://www.cell.com/biophysj/fulltext/S0006-3495(26)00041-X


