近日,进化所张伟鹏教授和海洋生命学院丁维副教授在iMeta杂志发表题为“Bioprospecting of culturable marine biofilm bacteria for novel antimicrobial peptides”(从可培养的海洋生物被膜细菌中发掘新型抗菌肽)的研究论文,通过使用新的方法对海洋生物被膜抗菌肽产生潜力进行了勘探,扩展了抗菌肽化合物的范围,为抗菌药源分子的研发提供了新视角。
抗生素耐药性已经成为一个重大的公共卫生威胁,寻找新型抗菌药物是抵御耐药细菌的一种重要方式,其中抗菌肽作为新型抗生素的一种潜在药物,受到广泛关注。抗菌肽是动物、植物和微生物产生的两亲性小分子多肽,具有广谱抗菌效果。在海洋环境中,生物被膜是附着在任何浸没基质上的微生物群落,如人造基质、石头表面、微塑料或动物内脏,生物被膜细菌因其独特的生态位和代谢特征,具有发现新型抗菌肽的巨大潜力。本研究聚焦于从可培养的海洋生物被膜细菌中发掘新型抗菌肽。
本研究从海洋生物被膜中进行了细菌菌株分离并对它们的基因组进行测序,构建了一个可培养的海洋生物被膜细菌库,包括713个菌株及其接近完整的基因组,为挖掘抗菌肽奠定了基础。随后,使用核糖体分析(Ribo-seq)与深度学习模型相结合的新方法预测抗菌肽,Ribo-seq分析的引入增强了序列过滤过程,使得在抗菌肽预测之前能够更准确地识别小开放阅读框(sORFs)。然后构建了一个由卷积神经网络、双向长短期记忆层和注意力层组成的深度学习模型,在80,430个表达的sORFs中鉴定出341个为候选抗菌肽,其中多数与公共数据库中的抗菌肽相似性低于40%,表明深度学习模型捕获了海洋抗菌肽的内涵特征。化学合成的60个候选抗菌肽中90%(54个)展示出抗菌活性,对多种人类耐药病原菌有强抑制作用。对其中12个强效抗菌肽进行的细胞毒性和溶血性测试显示了较低的毒性。最后,通过AlphaFold2预测和圆二色谱法探究抗菌肽结构,扫描电子显微镜和共聚焦激光扫描显微镜观测抗菌肽的作用靶点,揭示4种强效候选抗菌肽靶向金黄色葡萄球菌的细胞膜的杀菌机制。
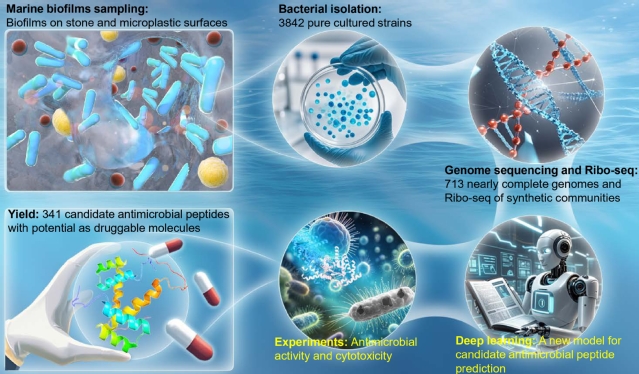
工作流程图
这项研究成功将Ribo-seq分析与新的深度学习算法相结合,从纯培养的海洋生物被膜细菌中预测出抗菌肽,并最终鉴定出与已知抗菌肽序列相似度低、性质不同的高效、低毒抗菌肽,为抗菌药源分子的研发提供了新视角。

张伟鹏老师实验室合影(后排右三张伟鹏教授)
中国海洋大学博士研究生范燊、秦澎、卢洁、王帅涛、张杰为该论文共同第一作者,张伟鹏教授和丁维副教授为共同通讯作者。相关工作得到山东省科研基金、中央高校基本科研业务费专项基金等资助。


