真核生物的基因表达通过组蛋白修饰与染色质重塑之间的相互作用实现动态调控,但这两者如何协调运作仍不完全清楚。近日,高珊教授课题组在Nucleic Acids Research杂志发表题为“Bromodomain protein IBD1 bridges histone acetylation and H2A.Z deposition to fine-tune transcription(溴结构域蛋白IBD1连接组蛋白乙酰化与H2A.Z添加从而精准调控转录)”的研究成果。

该研究以单细胞真核模式生物嗜热四膜虫(Tetrahymena thermophila)为体系,发现IBD1的溴结构域可特异性识别H3K9/K14双乙酰化修饰(H3K9/K14ac),并招募SWR复合体组分蛋白ARP6,从而促进组蛋白变体H2A.Z被精准添加至染色质中。当“组蛋白乙酰化-IBD1-H2A.Z”这一调控轴受到扰动时,会引发基因的异常高表达,表明H2A.Z在基因表达调控上具有双重功能:在维持基础转录水平的同时,抑制转录异常激活(图1)。这一发现为深入解析H2A.Z的生物学功能提供了新数据,也为理解染色质修饰与组蛋白变体在基因表达调控中的协同机制提供了新视角。
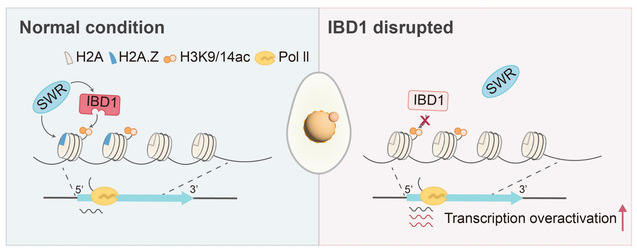
图1. 溴结构域蛋白IBD1调控转录稳态的模式图。
在四膜虫中,H2A.Z仅分布于转录活跃的大核,富集于转录活跃的基因区域,尤其偏向基因5′端,并与基因表达水平呈正相关(图2)。这提示H2A.Z与转录活跃密切相关,也为后续解析其调控功能提供了基础。
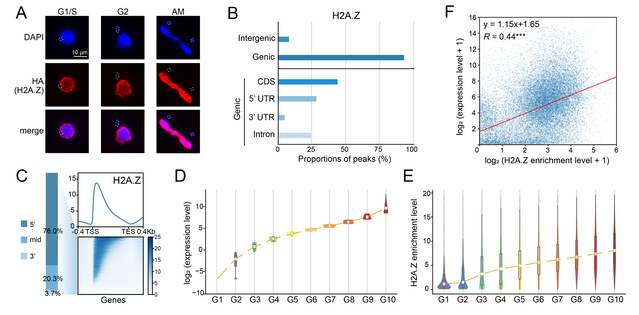
图2. H2A.Z富集与转录活跃相关。(A)H2A.Z特异性定位于大核;(B)H2A.Z主要富集于基因区;(C)H2A.Z倾向于富集在基因区的5′端;(D-E)基因按照WT中的表达水平由低到高分为G1-G10组,分别展示10组基因的表达水平和H2A.Z富集水平;(F)H2A.Z富集水平与基因表达水平呈正相关。
进一步的序列与功能分析显示,IBD1含有保守的溴结构域(bromodomain,BRD),该结构域能够识别组蛋白乙酰化修饰。当BRD发生突变(IBD1-BRDmut)时,IBD1在基因5′端的富集明显下降(图3A,D);而无论是IBD1缺失(ΔIBD1)还是BRD突变,都会导致ARP6在基因5′端的富集下降(图3A,B),由于ARP6是负责H2A.Z添加的SWR复合体的组分蛋白,这一变化进一步导致H2A.Z在基因5′端的分布下降(图3A,C)。
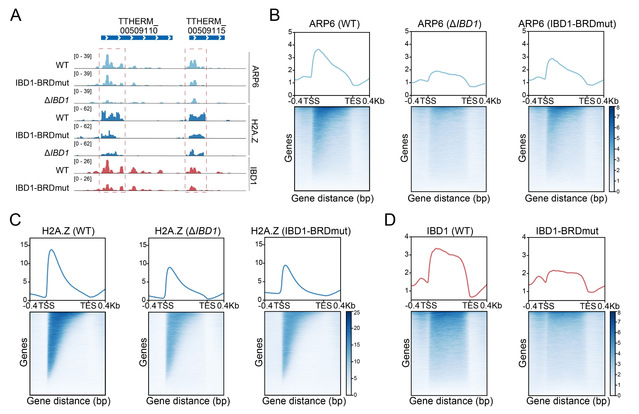
图3. IBD1的溴结构域介导H2A.Z的添加。(A)代表性基因位点上ARP6、H2A.Z和IBD1的分布;(B-C)ΔIBD1和IBD1-BRDmut中,ARP6和H2A.Z在基因区5′端的富集均降低;(D)IBD1-BRDmut中,IBD1在基因区5′端的富集降低。
团队随后探究了IBD1所识别的组蛋白乙酰化底物,发现IBD1偏好性识别H3K9/K14双乙酰化(H3K9/K14ac)(图4A)。H3K9/K14ac与H2A.Z的基因组分布特征也高度相似,倾向于分布在基因区5′端(图4B-C);同时,IBD1、H2A.Z以及H3K9/K14ac富集的基因也高度重叠(图4D)。将H3K9突变为Q(H3K9Q-RS)后,IBD1、ARP6以及H2A.Z的基因区5′端分布均降低(图4E-G)。
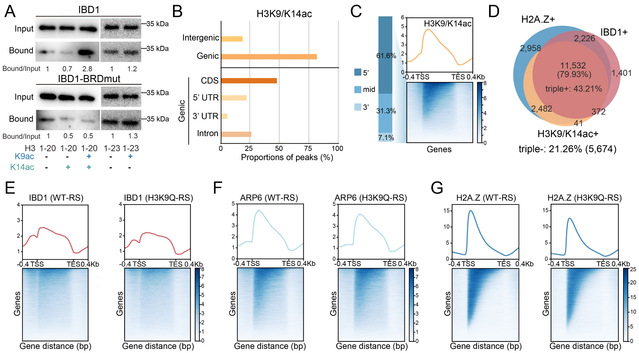
图4. 组蛋白乙酰化通过溴结构域介导的识别促进H2A.Z在染色质上的添加。(A)体外纯化的IBD1蛋白通过BRD偏好性识别H3K9/K14ac;(B)H3K9/K14ac主要富集于基因区;(C)H3K9/14ac倾向于富集在基因区的5′端;(D)H2A.Z(H2A.Z+)、IBD1(IBD1+)和H3K9/K14ac(H3K9/K14ac+)富集的基因高度重叠;(E-G)H3K9Q-RS中IBD1、ARP6和H2A.Z在基因区5′端的富集均降低。
进一步研究发现,IBD1功能受损(ΔIBD1或BRDmut)会引起广泛的转录上调,并伴随H2A.Z的基因区5′分布整体下降(图5A;图3C);ARP6敲低(ARP6-KD)也产生类似的广泛转录上调(图5A-B)。此外,H2A.Z、IBD1、H3K9/K14ac与Pol II转录基因的表达水平呈正相关(图5C);同时,H2A.Z与H3K9/K14ac的富集水平彼此呈正相关,且二者均与较高的转录活性相关。特别是在同时富集IBD1、H3K9/K14ac和H2A.Z(triple+)的基因中,IBD1缺失或BRD突变会导致H2A.Z分布显著下降并伴随转录明显升高(图5D-G)。这种变化在高表达基因中更为突出:H2A.Z下降幅度更大,转录上调也更为明显。这些结果表明,H2A.Z不仅与转录活性正相关,还在高乙酰化基因中发挥抑制转录过度激活的重要作用。在表型方面,这种转录失调带来了严重的生理影响:ΔIBD1和IBD1-BRDmut细胞生长速率相较野生型大幅度下降。
综上,该研究建立了新的分子调控通路:IBD1通过其溴结构域识别组蛋白乙酰化(尤其是H3K9/K14ac)被招募至染色质,随后介导SWR复合体(ARP6)在基因区5′端添加H2A.Z,从而维持转录稳态与细胞正常生长。
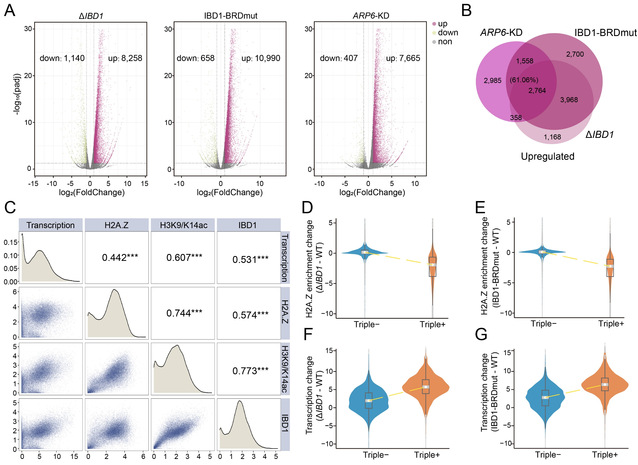
图5. H2A.Z与组蛋白乙酰化协同调控转录并防止过度激活。(A)ΔIBD1、IBD1-BRDmut和ARP6-KD中,转录大范围上调;(B)ΔIBD1、IBD1-BRDmut和ARP6-KD中转录上调的基因高度重叠;(C)H2A.Z、IBD1、H3K9/K14ac富集水平与基因表达水平呈正相关;(D-E)ΔIBD1和IBD1-BRDmut中,同时富集H2A.Z、IBD1和H3K9/K14ac的基因(triple+)以及缺失这三种标记的基因(triple-)的H2A.Z富集变化;(F-G)ΔIBD1和IBD1-BRDmut中,triple+与triple-基因的转录水平变化。
该研究由进化所原生动物学团队高珊教授课题组完成。高珊教授课题组博士生张喆、李海程,以及硕士毕业生鞠艾利为该文章的共同第一作者,王媛媛副教授和高珊教授为文章的通讯作者。高珊教授课题组博士毕业生叶飞,魏帆,刘永强,博士生牛俊骅,硕士生蒋泓桢对该工作亦有重要贡献。
原文链接https://academic.oup.com/nar/article/54/4/gkag148/8494756
参考文献:
1.Wong, L.H. and Tremethick, D.J. Multifunctional histone variants in genome function. Nat Rev Genet. 2025; 26: 82-104.
2.Strahl, B.D. and Allis, C.D. The language of covalent histone modifications. Nature. 2000; 403: 41-45.
3.Kouzarides, T. Chromatin modifications and their function. Cell. 2007; 128: 693-705.
4.Giaimo, B.D., Ferrante, F., Herchenröther, A., Hake, S.B. et al. The histone variant H2A.Z in gene regulation. Epigenetics Chromatin. 2019; 12: 37.
5.Billon, P. and Côté, J. Precise deposition of histone H2A.Z in chromatin for genome expression and maintenance. Biochim Biophys Acta Gene Regul Mech. 2012; 1819: 290-302.
6.Zhang, Z., Ju, A.L., Wang, Y.Y., Jiang, H.Z. et al. Bromodomain-containing proteins in the unicellular eukaryote Tetrahymena thermophila. Zool Res. 2025; 46: 538-550.
7.Saettone, A., Garg, J., Lambert, J.P., Nabeel-Shah, S. et al. The bromodomain-containing protein Ibd1 links multiple chromatin-related protein complexes to highly expressed genes in Tetrahymena thermophila. Epigenetics Chromatin. 2018; 11: 10.


